ELISPOT檢測的質量控制
那么如何能控制ELISPOT檢測的質量呢?如果有一種細胞和一種刺激物,并且ELISPOT斑點頻率是已知的話,那么就有了一個ELISPOT的標準系統。每次其它樣品檢測時,只要帶上這個系統,實驗者就可以用標準系統來質控待測樣品的ELISPOT檢測。這也是所有其它檢測質控的基本原理。
現在的關鍵是找到這樣一種細胞和一種刺激物,每次都能做出完全相同的ELISPOT結果。
二、標準細胞必須采用凍存細胞庫
首要問題是細胞。我們知道,細胞是有生命的,不像無生命的物質那樣容易保存。那么能不能采用新鮮細胞呢,比如每次都從同一個志愿者身上采集?不能。因為志愿者的健康狀態和**狀態都是動態的,雖說采自同一個人,但是細胞**水平可能會有變化,ELISPOT結果無法完全重復。那么能不能采集細胞之后長期飼養呢?不能。且不說長期培養成本高且周期長,細胞本身的**水平和克隆數目都會隨著培養和傳代而發生變化。
能滿足ELISPOT檢測長期不變化的只能是凍存細胞庫。一次采集大量細胞凍存在-197°C的液氮環境中,細胞的斑點頻率可以在數年之內恒定不變。PBMC分離和凍存復蘇的方法參見本網站內容。
三、標準刺激物選用CEF或者ICE
那么,刺激物選擇什么呢?非特異性的刺激物很便宜,但是不能用于質控。三個原因阻礙了這一點。
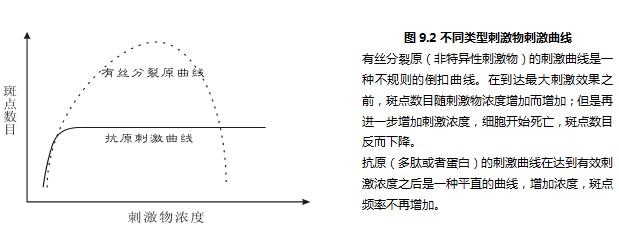
其一、非特異性的刺激物刺激效果不穩定。如圖9.2所示,非特異性的刺激物(有絲分裂原Mitogen)的刺激曲線幾乎沒有平坦的部分。也就是說,刺激物的濃度有細微變化,馬上就會體現在刺激斑點數目的變化上了,這樣實驗結果很難完全重現。相反,抗原的刺激曲線非常平坦,只要達到有效刺激濃度,斑點頻率就不再變化。
其二,非特異性刺激物的刺激原理與特異性的刺激物刺激原理不同。一般來說,質控系統和被質控的體系之間越相近越好:經過相同的處理,接受相同的影響因素,發生相同的物理、化學、生物過程。但是非特異性刺激物刺激是單細胞過程,與抗原經APC呈遞而刺激T細胞是完全不同的過程。所以用非特異性刺激反應質控與特異性刺激反應質控,從原理上也說不同。
其三,非特異性刺激物多數是蛋白質,比如PHA與ConA,效價不穩定,容易失活,不易保存。相對而言,作為抗原的蛋白和多肽,**原性和刺激效果要穩定得多。
綜上所述,在質控系統中,標準刺激物宜選用抗原。抗原中,以T細胞表位肽組成*簡單,機理*清楚,結果*穩定,所以是優選。再則考慮到標準刺激物對健康人的T細胞也應該能刺激作用,所以國際上選定三種常見病毒CMV、EBV、Flu Viurs,把它們的32條T細胞表位肽集中起來,作為ELISPOT標準樣性刺激物CEF。另有簡化版的23條肽肽庫ICE(貨號CT370),更加實用。
四、實驗室內部質控與實驗室之間的質控以及國家質控體系
以上介紹了ELISPOT質控系統的原理與組成。現在來介紹一下質控系統的應用范圍。根據質控系統的應用范圍,可以分為以下三個層次。
*基本的層次是實驗室內部質控系統。比如一個實驗室有好幾組實驗人員,會在很長的時間內(一年或數年)做高質量的ELISPOT檢測。這就需要用到實驗室內部的質控系統。因為實驗室內部的條件相對穩定,管理相對統一,實驗室內部質控系統的技術目前已經非常成熟。達科為公司有整套建立實驗室內部ELISPOT質控系統的方案,已經幫國內數家實驗室建立了這一系統。實踐也證明了該系統有效可行,指控效果非常明顯。
**個層次是實驗室之間的質控系統。當今的科研有合縱連橫的趨勢,一些重大的科研項目或者疫苗的臨床評估往往是跨實驗室、跨地域甚至跨國家的聯合項目。為了使這些分布在不同地區不同時間的ELISPOT檢測有相同的標準和可信度,必須采用實驗室之間的質控系統。就我們達科為公司與國內十余家實驗室聯合作的評估而言,實驗室之間的質控存在**的一個非技術障礙,那就是凍存質控細胞的運輸問題。
凍存細胞*好能通過液氮運輸,如果采用小型背負式液氮罐,實驗者可以在同一城市的不同實驗室之間運輸凍存細胞,但是對于跨城市或者跨國家的長途運輸就不太可能了。液氮罐上飛機或者火車都是非法的。如果采用干冰運輸,凍存細胞的狀態和存活率就會打折扣。我們的研究表明,經過干冰運輸的細胞,存活率只有80%左右。并且干冰運輸的可靠性也不能完全得到保證,一旦干冰耗盡或者細胞未完全**冰包裹,細胞的存活率就會直線下降,甚至完全死亡。
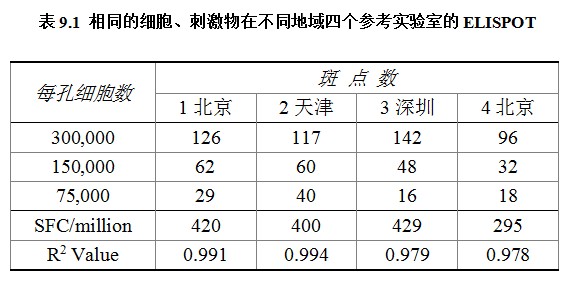
第三個層次是國家質控系統。任何成熟的檢測技術都會有相應過國家標準和質控系統。但是由于ELISPOT技術還在發展中,目前世界上還沒有任何一個國家建立了ELISPOT技術的國家標準和質控系統。美國是該項工作開展得比較早的國家,目前仍然在不同實驗室之間作驗證工作,研究建立質控系統的可行性。
如表9.1所示,這是我們一次實驗的結果。可以看到,前三個實驗室的結果重復性很好,但是第四個實驗室的結果明顯偏小。